Banebrytende hiv-forskning:
Slik saumfarte forskerne cellene fra «Oslopasienten»

Nordmannen som trolig er kurert for hiv skapte medieoverskrifter tidligere i år. Flere forskningsteam på OUS har samarbeidet om «Oslopasient»-prosjektet - og Mari Kaarbø ledet ett av dem.
Mari Kaarbø ble koblet på «Oslopasient»-prosjektet bare en måned etter at pasienten ble benmargstransplantert i 2020 (se rammetekst). Fra da av har hun hatt hovedansvaret for at pasientens blod- og tarmceller ble saumfart nøye i jakten på hiv-reservoarer. Hun har analysert selv (blant annet hele romjula 2024) og hun har samarbeidet med andre forskningsteam på OUS – og med utenlandske laboratorier.
- Vi har aldri hatt en pasient i Norge før som tilsynelatende er kurert for hiv. Vi hadde derfor ikke etablert alle nødvendige analyser. Men på IrsiCaixa AIDS forskningsinstitutt i Barcelona i Spania har de det. Der samler de inn og analyserer kliniske data og prøver fra hiv-positive pasienter som gjennomgår stamcelletransplantasjon. Vi samarbeider også med Aarhus Universitetsykehus i Danmark, der de i tillegg har etablert analyser for funksjonelt hiv-reservoar, forteller Kaarbø.
Hun ble utdannet bioingeniør ved Høgskolen i Østfold i 1998 og har etterpå tatt en master og en doktorgrad ved Griffith University i Australia. I dag er hun leder for Virologisk forskningsgruppe ved Avdeling for mikrobiologi, OUS.
Digital droplet PCR: Svært sensitiv
Både Kaarbøs lab og labene i Barcelona og Århus anvender såkalt digital droplet PCR (ddPCR) for å finne hiv-reservoar, en svært sensitiv metode, mye mer sensitiv enn vanlig kvantitativ PCR, kan Kaarbø fortelle. Med ddPCR deles DNA-prøven opp i titusenvis av små dråper, der hver dråpe er en separat PCR-reaksjon.
- Etter amplifikasjon kan man se hvilke dråper som er fluorescerende og inneholder målsekvensen - og hvilke som ikke gjør det. Slik kan man regne ut absolutt antall kopier, forklarer hun.
Kaarbø målte selv totalt hiv-DNA (både defekte og intakte provirus) i prøver som var tatt jevnlig etter transplantasjonen og to år fremover i tid. Laboratoriene i Barcelona og Aarhus analyserte i tillegg intakte provirus med Intact Proviral DNA Assay (IPDA), der man måler to ulike regioner i virusgenomet samtidig. Bare provirus som har begge regionene intakte regnes som potensielt funksjonelle, mens de fleste andre er defekte.
På den måten får man både et mål på den totale mengden hiv-DNA - og hvor stor andel som faktisk kan være replikasjonsdyktig, forklarer hun.
- Vi har ikke hatt behov for å utføre IPDA her tidligere, vi hadde jo ingen pasienter det var aktuelt å bruke den på. Men nå skal vi innføre analysen. Vi ønsker også å benytte den i andre hiv-relaterte prosjekter, forteller hun.
Mutasjonen som overlevde svartedauden
Det er CD4-cellene som blir angrepet av hiv. Via CD4-resptoren og koreseptorene CCR5 eller CXCR4, som sitter på overflaten av cellene, fester viruset seg og trenger inn i cellene der det lager nye kopier. Men det finnes personer som er immune mot viruset. De har en mutasjon i CCR5 som enten gjør dem helt immune (hvis mutasjonen er homozygot) eller bedre beskyttet (heterozygot). I Norge er ikke denne mutasjonen helt uvanlig. Om lag 15 prosent har den heterozygote mutasjonen mens rundt 1,5 prosent har den homozygote.
- Man tror at en stor epidemi, muligens svartedauden, er årsaken til at en såpass stor andel har mutasjonen i Nord-Europa. De som hadde den, hadde trolig også større sjanse til å overleve. I land der epidemien ikke rammet like hardt, er andelen med mutasjonen langt lavere, forteller Kaarbø.
På jakt etter hiv med digital droplet PCR (ddPCR)



Broren til «Oslopasienten» tilhører altså de 1,5 prosentene som er immune mot hiv. At han i tillegg hadde samme vevstype som broren er et lite under. Sannsynligheten for det var uhyre lav.
Aferese i Århus
For å undersøke om «Oslopasienten» fortsatt hadde replikasjonsdyktig virus, ble han sendt til Århus i Danmark for aferese. Der benyttet laboratoriet metoden «Quantitative viral outgrowth assay» (QVOA) for å måle mengden replikasjonsdyktig hiv som kunne finnes skjult i latente celler. Kaarbø forklarer:
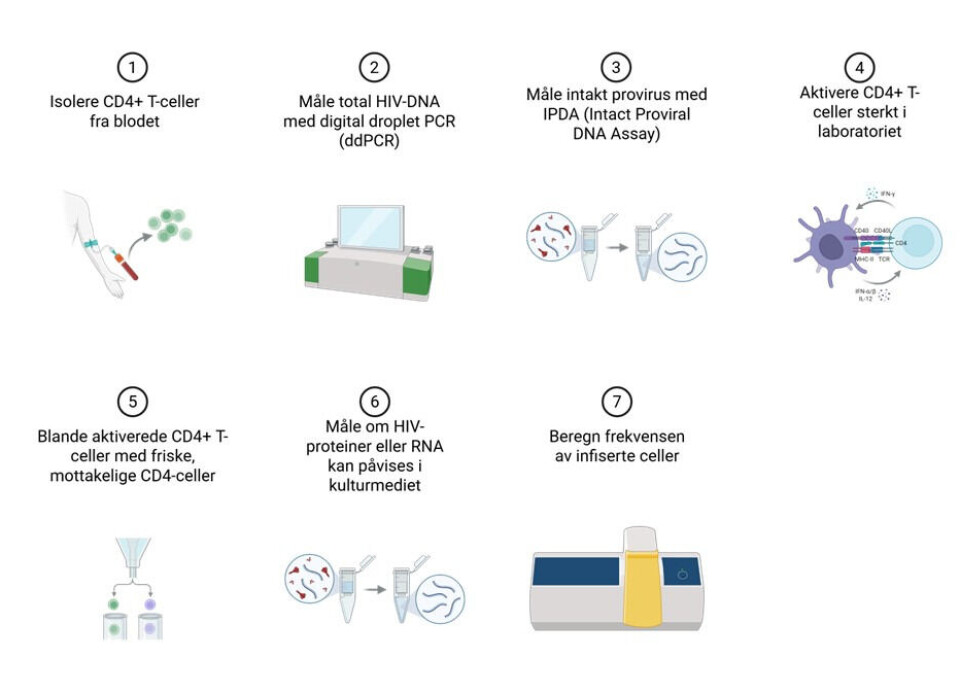
- Man isolerer først CD4+ T-celler fra blodet og aktiverer dem, slik at eventuelle latente provirus begynner å produsere virus. Disse cellene blandes så med friske, mottakelige CD4-celler som fungerer som matceller. Viruset kan dermed spre seg hvis det er funksjonelt. Etter noen dagers dyrking måler man om hiv-proteiner eller RNA kan påvises i kulturmediet. Antall positive brønner brukes til å beregne frekvensen av infiserte celler. Kort sagt: QVOA tester ikke bare om hiv-DNA er til stede i cellene, men om det faktisk kan gi opphav til nytt, smittsomt virus.
- Hvorfor ble det brukt aferese?
- Fordi man til QVOA trenger mange millioner CD4-celler. Og siden denne celletypen kun finnes i små mengder i blodet, holder det ikke å ta en vanlig blodprøve. Ved aferese tapper man blod fra kroppen, tar ut den celletypen man trenger, og så føres resten av blodet tilbake. På den måten kan man hente ut store mengder CD4-celler uten å tappe kroppen for mye blod.
Resultatet av alle analysene, utført i Oslo, Barcelona og Århus, var at det ikke fantes aktivt virus verken i pasientens blod eller tarm.
Deteksjon av hiv-reservoaret
Presenterte resultater på gigakonferanse
Kaarbø og de andre lederne i prosjektet presenterte resultatene sine på CROI-konferansen (Conference on Retroviruses and Opportunistic Infections, verdens største hiv-forskningskonferanse) i San Francisco i mars. Det var et gigantisk arrangement med rundt 6000 deltakere, forteller hun.
- Siden vi ennå ikke har publisert funnene, presenterte vi en del av resultatene på poster.
Men resultatene skal snart publiseres – ifølge Kaarbø i et høyt rangert vitenskapelig tidsskrift. Hvilket, vil hun ikke røpe.
Mer forskning?
Men hva skjer nå? Forskerne har stadig kontakt med «Oslopasienten», som fremdeles er frisk og fornøyd. Men kan han og cellene hans brukes til enda mer forskning? Er det mulig å finne en kur mot hiv/aids?
Kaarbø forteller at hun gjerne skulle hatt tarmbiopsier tatt før benmargstransplantasjonen. Da kunne hun ha sammenliknet tarmceller før og etter. Det hun kan gjøre, er å sammenligne funnene hos «Oslopasienten» med andre grupper, blant annet for å finne ut om pasienten er kurert for alltid.
- Vi kan sammenligne med personer som lever med hiv og får vanlig behandling. Hos dem finnes det som regel små virusrester og intakt hiv-DNA igjen i blod og tarm. Vi kan også sammenligne med en sjelden pasientgruppe som holder viruset nede helt uten medisiner, såkalte elitekontrollører. Og vi kan se på andre, både med og uten hiv, som har fått stamcelletransplantasjon. Da kan vi kanskje skille mellom hva som skyldes selve transplantasjonen og hva som handler om viruset.
- Dagens behandling av hiv-pasienter er god. De kan leve lange og symptomfrie liv uten å være smittsomme. Er det likevel viktig å finne en behandling som kurerer?
- De fleste pasienter som lever med hiv kan leve helt normale liv, det er riktig – men, de må ta medisin hver dag resten av livet for å holde viruset i sjakk. Hvis de slutter, kan virusreservoaret aktiveres og føre til aids. Derfor er håpet å finne en kur som gjør at man kan leve og være frisk - helt uten medisiner, sier Mari Kaarbø.


























