FAG Essay
Epigenetikk - bindeleddet mellom arv og miljø
Det har lenge vært enighet om at en kombinasjon av arv og miljø påvirker personligheten og de kroppslige egenskapene våre. Gjennom studier av det som kalles epigenetikk, har forskerne de siste årene funnet ut stadig mer om hvordan miljøet påvirker genene våre.
Da The Human Genome Project ble publisert i Nature i 2003, var det mange som undret seg. Det viste seg nemlig at det menneskelige genom bare inneholder et sted mellom 20 000 – 25 000 gener. En risplante inneholder jo 50 000 gener, hvordan kan en så biologisk avansert organisme som et menneske da inneholde så få gener? De neste årene viste imidlertid at selv om vi mennesker har få gener, har vi en fantastisk kompleksitet i hvordan vi regulerer genene våre. Epigenetikk er et forholdsvis nytt forskningsfelt som er en av flere mekanismer som er involvert i denne genreguleringen.
Epigenetikk betyr på latin over eller ved siden av genetikken, og beskriver hvordan gener aktiveres eller inaktiveres. Hvert enkelt gen kan ha flere kjemiske grupper festet til seg som virker som av- og på-knapper. Noen kjemiske grupper kan være tilstede i en kort periode, mens andre kan sitte på genet i lange perioder, noen ganger hele livet. På den måten overstyres informasjonen i selve DNA-sekvensen i genet, siden epigenetikken bestemmer om genet er aktivt eller ikke. Ytre påvirkninger som kosthold, trening, røyking og ekstrem frykt, ser ut til å kunne påvirke genaktiviteten.
Med de nye DNA-sekvenseringsteknikkene er det mulig å sekvensere personlige genomer som kan gi informasjon om alle sykdommer vi er disponert for gjennom genene. Det er imidlertid ikke nødvendigvis gitt at man utvikler en bestemt sykdom selv om man har en genmutasjon som forårsaker denne sykdommen, fordi miljømessige eller epigenetiske faktorer påvirker hvordan dette genet uttrykkes. Takket være den enorme teknologiske utviklingen i avlesing av hvilke kjemiske grupper som er festet på DNA, har forståelsen for epigenetikk og helse økt innen medisinsk forskning de siste fire-fem årene
Arv eller miljø?
Epigenetikk har tatt den gamle debatten om hva som påvirker oss mest i utviklingen fra barn til voksen, arv eller miljø, et skritt videre. Mange husker kanskje den populærvitenskapelige tv-serien «Hjernevask», hvor Harald Eia debatterte om miljøet eller genene har størst betydning for hvordan vi utvikler oss fra barn til voksen.
Vi vet at en del trekk hovedsakelig er bestemt av gener. Dette har man funnet ut ved å studere eneggede tvillinger, som har identiske gener, siden de har utviklet seg fra et befruktet egg som har delt seg i to, rett etter befruktning. Fra disse studiene vet vi at trekk som øyefarge er bestemt av gener. Har et embryo genene for brune øyne, vil barnet få brune øyne – uavhengig av hva slags miljø det vokser opp i.
På samme måte er det med enkelte arvelige sykdommer, som Huntingtons sykdom. Har man genmutasjonen som gir sykdommen, blir man garantert syk. På den annen side er andre trekk i all hovedsak bestemt av miljø, som kulturforståelse og læring av språk. Et barn lærer ikke kinesisk hvis det ikke har en person i nærmiljøet som kan lære barnet språket. Men de fleste forskere er i dag enige om at de fleste trekk er et samspill mellom arv og miljø. Og epigenetikken er et forskningsfelt som bygger bro mellom arv og miljø, og går inn på detaljnivå på genene våre og ser på hvordan gener slås av eller på i respons på signaler fra miljøet.
Hva er epigenetikk?
Begrepet epigenetikk ble først beskrevet av den britiske forskeren Conrad Hal Waddington i 1942. Han brukte Aristoteles’ begrep epigenesis til å beskrive hvordan gener i Drosophila melanogaster, bananfluer, kan endre uttrykk når de utsettes for ytre stress. Dette var ti år før strukturen til DNA-dobbeltheliksen ble publisert, og Waddington hadde naturlig nok ingen molekylærbiologisk forklaring på fenomenet. Teorien hans var kontroversiell i sin tid, men i dag vet vi at forklaringen er at ytre stress fikk genene i bananfluen til å endre aktivitet takket være epigenetisk regulering.
DNA i en menneskecelle er tett pakket sammen, og det essensielle i epigenetikk er at aktiviteten til genene reguleres ved at pakkingen av DNA endres. DNA kveiler seg rundt et proteinkompleks bestående av åtte histonproteiner; fire ulike histoner (H2A, H2B, H3 og H4) med to av hver, som til sammen danner en oktamer. Dette er den minste pakkeenheten og kalles et nukleosom. DNA kveiler seg to ganger rundt nukleosomet, dette utgjør 146 basepar. Pakkingen av DNA rundt histonene beskytter DNA for mekanisk skade, samtidig som graden av pakking bestemmer aktiviteten til genet.
Graden av pakking bestemmes blant annet av epigenetikk; kjemiske grupper som påvirker pakkingen av DNA rundt histonene. For at et gen skal være aktivt, må enzymene som skal avlese informasjonen i DNA, inkludert RNA-polymerasen med hele sitt maskineri, få tilgang på DNA-tråden. Hvis DNA er åpent og tilgjengelig, er genet aktivt. Selv om DNA er aktivt, er arvestoffet fremdeles pakket rundt histonene, men har en løsere struktur. Dersom DNA er tett pakket får ikke enzymene tilgang, og genet er inaktivt.
De kjemiske gruppene som er de epigenetiske merkelappene, kan enten feste seg på selve DNA-tråden, eller til endene på histonene som stikker ut. Den mest kjente kjemiske gruppen er en metylgruppe som får DNA til å pakkes tett sammen. Metylering inaktiverer dermed genene. Metylgrupper fester seg hovedsakelig til CpG-øyer i promotorområdet til genet, men kan også feste seg i selve genet eller i andre regulatoriske sekvenser. Andre eksempler på kjemiske grupper er acetylgrupper, som får DNA-strukturen til å åpne seg og dermed aktiviserer gener.
Det er et stort, komplekst apparat med flere grupper enzymer som er involvert i påsetting, registrering og fjerning av de kjemiske gruppene (figur 1).
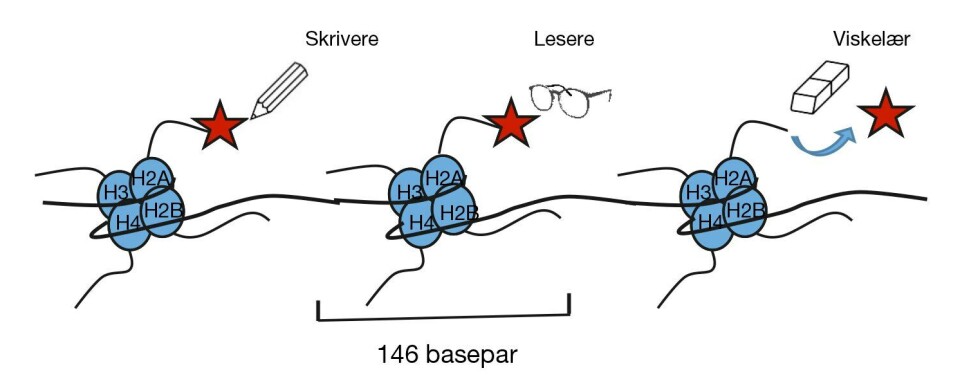
Som en metafor på prosessen kan man tenke seg at enzymene som setter på de kjemiske gruppene enten virker som kulepenner eller blyanter. Kulepennene setter på kjemiske grupper som blir sittende fast og kan være tilstede hele livet. Hvis det skjer i kjønnscellene kan den epigenetiske modifikasjonen overføres til neste generasjon. Enzymene som virker som blyanter setter de kjemiske gruppene løst på, og de kan dermed lett viskes bort.
I tillegg til kjemiske grupper er RNA-molekyler viktige i det epigenetiske maskineriet. Den delen av arvematerialet vårt som ikke er gener og som forskere tidligere trodde var søppel-DNA, har vist seg å blant annet kode for RNA-molekyler som kan binde seg til gener og inaktivere dem. Et eksempel på dette, som finnes i de fleste organismer, er inaktivering av X-kromosomet hos hunnkjønn. Siden hunnkjønn har to X-kromosomer, inaktiveres det ene X-kromosomet i alle celler. Et stort RNA-molekyl legger seg rundt det ene X-kromosomet tidlig under embryoutviklingen, og inaktiverer alle genene på akkurat dette X-kromosomet. Inaktiveringen er permanent og vil vedvare hele cellens levetid og gis videre til nye celler ved celledeling. Det ser ut til å være tilfeldig hvilket X-kromosom som velges (1).
Et synlig eksempel på dette finnes hos Calico-katter, hvor genene som styrer pelsfargen ligger på X-kromosomet (XX). Siden hunnkatter har to X-kromosomer, inaktiveres et av X-kromosomene i alle kattenes celler, på en tilfeldig måte. Hvis hunnkatten har et X-kromosom som har genet for svart farge, og det andre X-kromosomet har genet som koder for orange farge, vil kattens pels være en blanding av svart og orange (figur 2).

Den samme inaktiveringen av det ekstra X-kromosomet skjer også hos mennesker. Noen ganger kan det skje at inaktiveringen av X-kromosomet skjer hovedsakelig i X-kromosomet fra enten mor eller far, såkalt skjev X-kromosominaktivering. Da kan typiske kjønnsbundne sykdommer som hemofili (blødersykdommer) og Duchennes muskeldystrofi, som vanligvis rammer gutter (fordi de har bare ett X-kromosom, og dermed mer utsatt for sykdommer som skyldes mutasjoner på X-kromosomet), også opptre hos jenter.
Viktig for fosterutviklingen
Det er epigenetikken som gjør at cellene i et tidlig embryo klarer å utvikle seg til alle de over 220 ulike celletypene vi har i kroppen. Rundt fem dager etter befruktningen, består embryoet av en struktur med om lag 250 celler som kalles blastocyst (figur 3). Blastocysten ser ut som et bringebær med store celler som omslutter et hulrom. Den ene enden av hulrommet inneholder stamcellene som skal utvikle seg til et helt individ. Disse identiske stamcellene er pluripotente, det vil si at de kan utvikle seg til alle kroppens celler i individet som skal fødes ni måneder senere.
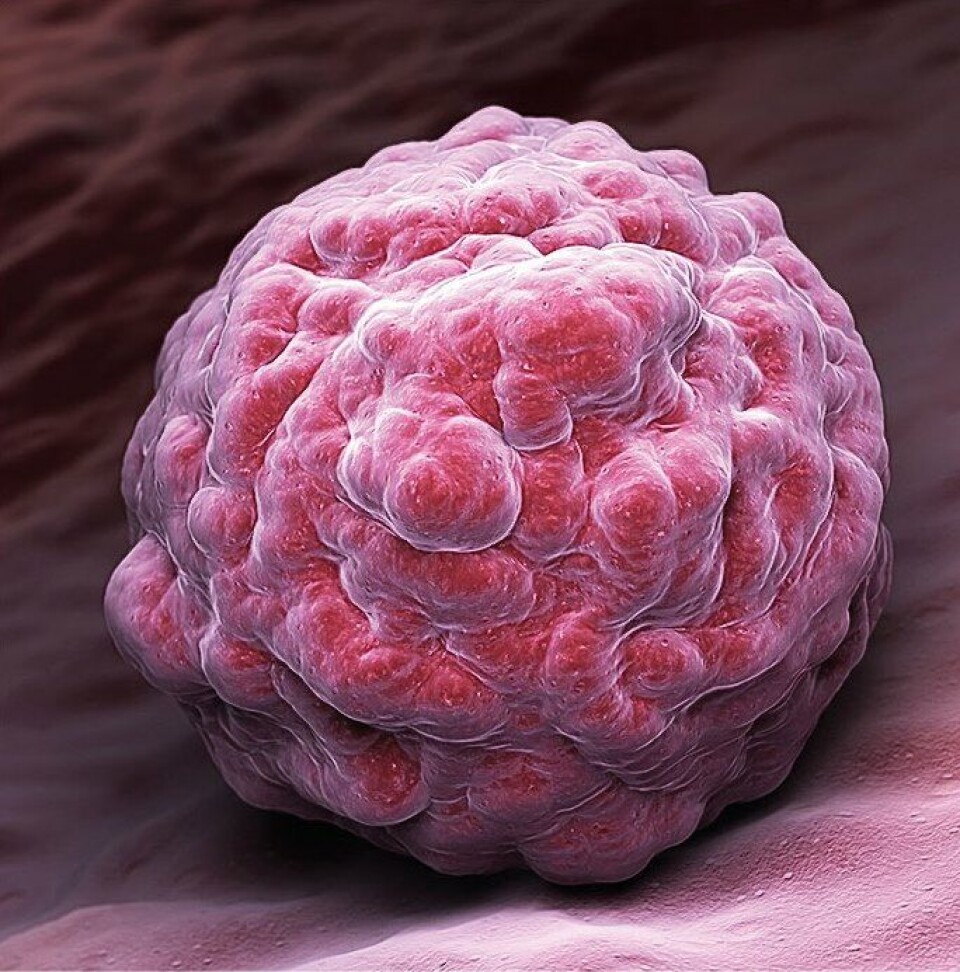
Siden alle kroppens celler utvikler seg fra disse stamcellene, betyr det at alle kroppens celler inneholder de samme genene, men har aktivert de genene som er nødvendige i det vevet cellene befinner seg i. Hudceller og nyreceller har identisk DNA, men i nyrene har cellene aktivert de genene som er nødvendige for at nyrene skal rense og skille ut urin, mens resten av genene er inaktivert. I hudcellene er genene som gjør at huden danner et beskyttende lag rundt kroppen aktivert, mens alle andre gener er slått av.
Ved å kombinere ny DNA-sekvenseringsteknologi med detaljert analyse av de ulike epigenetiske modifikasjonene, har det blitt mulig å lage epigenetiske kart som sier noe om hvilke gener som er skrudd på og hvilke som er skrudd av i forskjellige celletyper. Det viser seg at måten de epigenetiske modifikasjonene fordeler seg langs genomet (det såkalte epigenomet), varierer mellom ulike celletyper og ulike cellestadier. Selv om vi bare har ett genom som er relativt likt i alle cellene våre, har vi hundrevis av forskjellige epigenomer. Disse epigenomene forandrer seg gjennom utviklingen fra embryo til voksent menneske, ved miljøpåvirkning og fra celletype til celletype.
Mors kosthold kan påvirke embryoets gener
Et av de første studiene som viste at mors kosthold under graviditeten direkte kan endre epigenetikken til embryo, er en elegant studie i mus (2). En musestamme har et aktivt Agouty-gen, som gjør at de er overvektige, har gul pelsfarge og har økt risiko for sykdommer som diabetes og kreft (figur 4). Vanlig musefôr inneholder få metylgrupper, og ved å gi gravide Agouty-mus vanlig musefôr under graviditeten, føder hun unger som er gule, overvektige og syke. Hvis derimot den gravide musemoren får musefôr som inneholder større mengder metylgrupper i fôret, i dette forsøket folat og vitamin B12, fester metylgruppene seg til Agouty-genet i museembryoene under fosterutviklingen og musene som fødes er slanke, brune og har ikke økt risiko for sykdommer. Metylgruppene fra mors mat har inaktivert Agouty-genet i museembryoene.

Mange miljøfaktorer kan påvirke epigenomet
I løpet av de siste årene har det kommet mange studier som viser at for eksempel stress, kosthold og temperatur kan påvirke epigenetikken i cellene våre – og i noen tilfeller også i kjønnscellene, så endringene overføres til fremtidige generasjoner. Ved å studere epigenetiske forskjeller (metyleringer og acetyleringer) i blodceller til eneggede tvillinger, viste en studie at det var få forskjeller i genreguleringen når tvillingene var små. Tre år gamle tvillinger hadde de samme genene aktivert, men jo eldre tvillingparene ble, jo større ble forskjellene (3). Hos 50 år gamle identiske tvillinger var forskjellen i den epigenetiske reguleringen stor, og forskjellene var størst hos de tvillingparene som hadde ulik livsstil og levde langt fra hverandre.
Kosthold er én av miljøfaktorene som kan påvirke de epigenetiske modifikasjonene av bestemte gener. Vi vet fra historiske studier at tilgang på næring under svangerskap påvirker fosteret. Et eksempel er fra vinteren 1944 da Nederland var okkupert av Tyskland. Tyskernes blokade av all forsyning førte til ekstrem hungersnød. Over fire millioner mennesker ble rammet og 22 000 mennesker sultet ihjel. Et stort forskningsprosjekt har fulgt de kvinnene som var i første trimester (frem til 12 uker) under hungersnøden. Da barna ble født, var krigen over, og til forskernes overraskelse hadde disse barna en større grad av overvekt enn resten av befolkningen. De hadde også økt risiko for sykdommer som diabetes og hjerte- og karsykdommer, og levde i snitt seks år kortere enn resten av befolkningen. Den påfølgende generasjonen fulgte det samme mønsteret: kortere livslengde og økt risiko for visse sykdommer (4, 5).
Epigenetikk ser ut til å være en del av forklaringen. Fra dyrestudier vet vi at når gravide mus får lite mat under svangerskapet, blir genene som styrer sult aktive i museembryoene. Metyleringsmønsteret endrer seg i disse genene. Hvis museungene får god tilgang på mat når de vokser opp, fører den økte sultfølelsen til at de spiser mer mat enn de trenger. Det samme gjelder for mennesker. En teori er at sult er noe av det farligste et menneske kan oppleve, derfor tilpasser embryoet seg og aktiverer sultgenene (6).
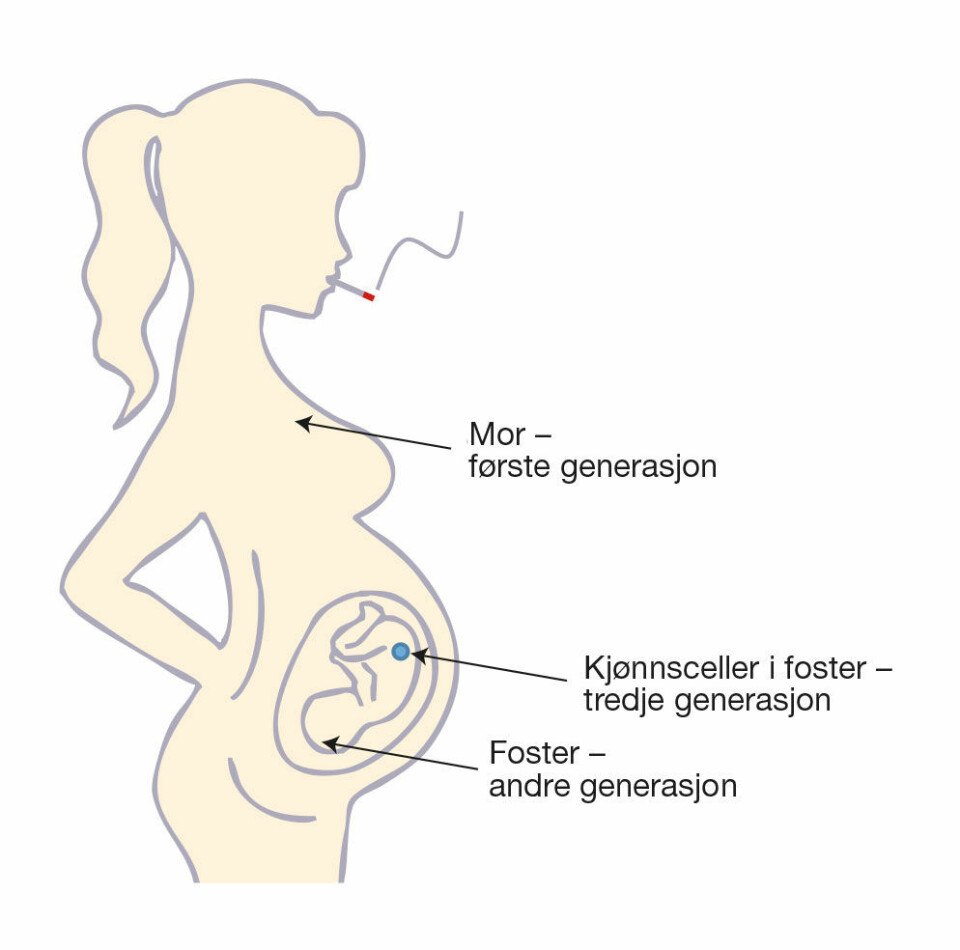
For noen år siden viste en annen studie fra svenske forskere at det var en sammenheng mellom frekvensen av diabetes, overvekt og livslengde hos barn - og om deres bestefedre og -mødre sultet tidlig i livet. Det interessante er at disse arvbare forandringene i fenotypen ikke gjenspeiler seg i forandringer eller mutasjoner i selve DNA-sekvensen til genene, kun i epigenetikken (7). På samme måte har flere studier vist at hvis mormor røykte under graviditeten, har barnebarna en 20 prosent økt risiko for å utvikle astma, sammenlignet med den øvrige befolkningen. Det er fordi nikotinet har laget permanente endringer i metyleringen i gener som er involvert i lungefunksjon, både i den gravide selv (mormor), og i hennes barn og barnebarn (figur 5) (8).
Epigenetisk arv kommer også fra far
Også fars kosthold ser ut til å påvirke hvilke epigenetiske knagger som settes på DNA-et i sædcellene. Hvis en mann er overvektig, fører det til at gener som styrer insulinresistens og overvekt aktiveres i sædcellene. Hvis han får barn, har barna derfor økt risiko for å bli overvektige og utvikle diabetes, siden de har de samme endrede metyleringsmønstrene i sine celler. Studier viser at genene i sædcellene kan være mest mottakelig for epigenetiske endringer rett før puberteten, når gutter er mellom ni og tolv år. Mye mat i denne perioden av livet gjør at kommende barn og barnebarn har økt sannsynlighet for å utvikle overvekt, få visse sykdommer og leve kortere enn resten av befolkningen. Andre faktorer som røyking, stress og eksponering for visse toksiner, påvirker også metyleringsmønsteret i sædcellene. Det er estimert at rundt 100 gener i sædcellene kan permanent endres epigenetisk på grunn av ytre påvirkninger (9).
Kan frykt gå i arv?
En studie på mus viste for noen år siden at frykt kan lage permanente endringer i metyleringene i kjønnscellene i hannmus, og dermed gis videre til neste generasjon (10). Hannmus fikk elektrisk støt under potene i fem dager. De elektriske støtene var ubehagelige og musene viste tydelig tegn på redsel. Samtidig som musene fikk støt kom det en sterk lukt av mandler inn i museburene (gitt som kjemikaliet acetophenone). Etter noen uker ble musene på nytt eksponert for mandellukt, og musene ble redde, selv om de denne gangen ikke fikk støt under potene. Musene forbandt lukten med de vonde, elektriske støtene. Hannmusene ble krysset med hunnmus, og museungene som ble født, hadde arvet farens redsel for mandellukt. Hver gang museungene kjente lukten av mandler, ble de redde, selv om de aldri har opplevd å få elektriske støt. Det samme skjedde med neste generasjon museunger. Da forskerne som gjennomførte studien analyserte hvilke gener som var endret i musene, fant de ut at gener som laget reseptorer for mandellukt var aktivert i musene. Det samme var gener som styrer frykt og nervøs adferd. Mus bruker luktesansen for å finne mat og unngå farer, og det er viktig å tilpasse seg endringer i miljøet raskt. Museunger kan dermed få en evolusjonær fordel ved at genene deres har fått med seg erfaringen fra foreldrene og besteforeldrene.
Det finnes også studier som viser at frykt kan lage permanente endringer i kjønnscellene hos mennesker. Foreldre som sliter med vedvarende angst og depresjon etter ekstreme opplevelser, som Holocaust og borgerkrigen i Rwanda, har genforandringer som kan overføres til barna og gjøre dem mer utsatt for lignende psykiske lidelse (11). Kritikken mot studiene er at de er små med få deltagere, og mer forskning behøves for å underbygge årsakssammenhengene.
Epigenetikk og aldring
Aldring er en komplisert biologisk prosess hvor normale fysiologiske funksjoner i kroppen gradvis slutter å virke. Fra studier på bier og mus vet vi at forskjellige miljøpåvirkninger som mat og trening påvirker epigenetikken og henger sammen med livslengden. Cellene blir gamle fordi epigenetikken gjør noen gener aktive og andre inaktive, slik at cellene fungerer dårligere. Det ser ut til at mange av de epigenetiske endringene som kommer gjennom et langt liv er reversible, og at enzymer som setter på og fjerner de kjemiske gruppene raskt kan aktiveres.
Flere studier som er publisert de siste par årene viser at biologisk alder og epigenetikk kan henge tett sammen. De epigenetiske forandringene som skjer i cellene våre etter hvert som vi blir eldre, ser ut til å gå saktere i mennesker som lever sunt. Det kan forklare hvorfor to personer som begge er 60 år, kan ha helt ulik biologisk alder. Trening, sunt kosthold og nok søvn ser ut til å forsinke den epigenetiske aldringsprosessen (12).
Medisiner som påvirker epigenetikken
Siden de fleste epigenetiske endringer er reversible, forskes det på å utvikle medisiner som kan endre metyleringen i genene. Kreftceller har for eksempel ofte et annet metyleringsmønster enn andre celler. Målet er å hemme kreftutvikling ved å utvikle medisiner som kan endre metyleringsmønsteret i kreftcellene tilbake til slik det opprinnelig var. En av fremtidens behandlinger mot kreft og andre sykdommer som diabetes, kan derfor være en epigenetisk medisin som skrur av og på helt bestemte gener.
Fremtiden
Epigenetikk er et forholdsvis nytt fagområde, og det er fremdeles mye vi ikke vet om hvordan miljøet rundt oss påvirker genene. I dag vet vi at vår fysiske helse er et resultat av genene vi har arvet fra mor og far, samt måten vi lever på. Røyking, fysisk aktivitet, kosthold, søvn og overvekt er viktige faktorer som bestemmer om vi holder oss friske eller blir syke. Selv om man for eksempel skulle ha økt risiko for å utvikle astma fordi mormor røyket under svangerskapet, vil antagelig sunn livsstil redusere risikoen betraktelig.
En gang i fremtiden vil det kanskje bli vanlig at bioingeniører analyserer blodprøver fra pasienter for å finne ut hvilke epigenetiske merkelapper som skyldes besteforeldrenes livsførsel. Videre kan de analysere hvor langt den epigenetiske aldringen er kommet. Dermed kan legen gi pasienten medisiner som kan forsinke den biologiske aldringsprosessen.
Mens vi venter på dette, får vi prøve å ta så gode livsstilsvalg som mulig, slik at de gode genene våre er aktive - og at de dårlige inaktiveres.
Intervju med artikkelforfatteren Elisabeth Larsen og bioingeniør Mari Kaarbø:
























