Fag i praksis
Ny og bedre metode for diagnostikk og oppfølging av nevroendokrine svulster
For vel et år siden startet OUS Rikshospitalet med ny og bedre metode for avbildning av nevroendrokrine svulster med bruk av PET-teknologi. Innmerking av radiofarmakonet 68Ga-DOTATOC gjør vi nå selv på Avdeling for Nukleærmedisin
Av AUD EMBLEMSVÅG MELBØE, bioingeniør med spesialistgodkjenning i nukleærmedisin, Enhetsleder Drift Nukleærmedisin, Oslo universitetssykehus Rikshospitalet
Ny og bedre metode for diagnostikk og oppfølging av nevroendokrine svulster.pdf(283 KB)
Tidligere avbildet vi nevroendokrine svulster med gammakamera eller SPECT/CT med bruk av radiofarmakaene 111In (Indium) - Octreoscan eller 99mTc (Technesium) – Tectrotyd. Det har lenge eksistert bedre metoder for avbildning av nevroendokrine svulster med anvendelse av PET-teknologi, men disse har ikke vært tilgjengelig i Norge. Da det kom en ny og enklere 68Germanium-/68Gallium-generator på markedet i 2018 åpnet det muligheten for at vi selv kunne produsere radiofarmaka til bruk for PET.
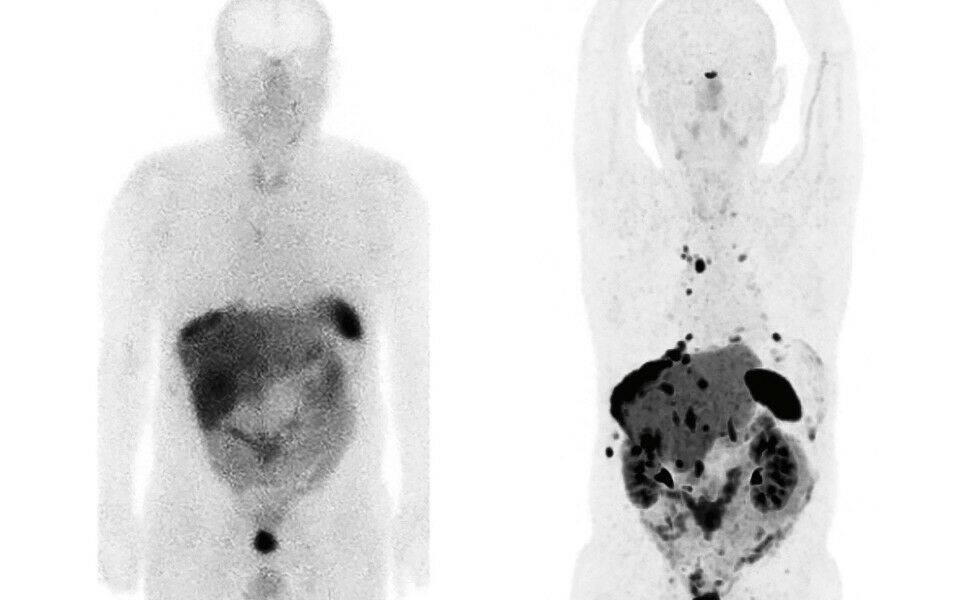
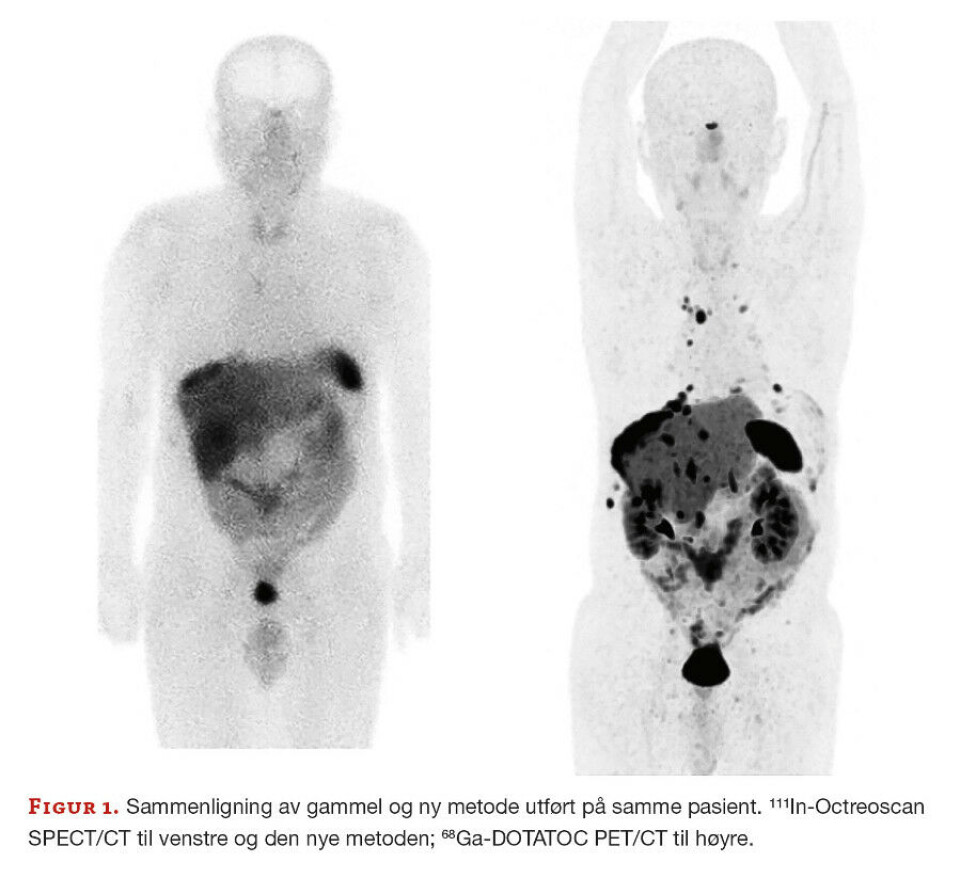
Den nye undersøkelsesmetoden er betraktelig bedre med høyere spesifikk bindingsevne til reseptorer på celleoverflaten i svulstvevet. PET-skannere er i tillegg over 10 ganger mer følsomme enn SPECT-skannere (figur 1).
Den nye metoden gir også en raskere og enklere undersøkelse for pasienten. Pasientene får nå utført hele undersøkelsen på cirka to timer, og ikke som tidligere der vi gjorde avbildninger over en til to dager med tarmtømming som en del av regimet. Pasienten får gjort både PET og CT i PET/CT-skanneren. Det gjør at bildene er direkte sammenlignbare og pasienten slipper å ta to adskilte undersøkelser.
Med den nye avbildningsteknikken ser vi utbredelse av sykdomsforløpet på et mye tidligere stadium. Vi ser også omfanget av spredning til ulike organer og vev tydeligere. Det har gitt et helt annet verktøy for klinikerne i diagnostisering og oppfølging av behandlingsforløpet.
I denne artikkelen vil jeg presentere hvordan vi utfører innmerking med den radioaktive isotopen 68Ga (Gallium) til den spesifikke biokjemiske forbindelsen DOTATOC, som binder seg til reseptorer på celleoverflaten av svulstvev og metastaser av nevroendokrin karakter. Videre legges det vekt på hvordan vi utfører kvalitetskontroll for å sikre at produktet har høy nok innmerkingsprosent av radioaktivitet, og ikke er bundet til andre forurensende substanser underveis i prosessen.
Nukleærmedisinske metoder
Prinsippet for nukleærmedisinske metoder er at vi merker en biologisk eller metabolsk substans med radioaktivitet; vi får da et radiofarmakon. Radiofarmakonet injiseres i pasienten og vil bindes biokjemisk eller tas opp i vev/organ eller en sykdomsprosess vi er interessert i å synliggjøre. Ved å bruke en radioaktiv isotop kan man registrere opptaket i pasienten med et nukleærmedisinsk kamera. Ved å samle nok stråler/tellinger over tid får vi et detaljert bilde av opptaket i aktuelle organer eller vev (1).
Gammaemittere og SPECT
SPECT står for Single Photon Emission Computed Tomography. Det er i prinsippet et gammakamera med en stor planar flate som er dekket med en Natriumjodid (NaI)-krystall. Bakenfor ligger det fotomultiplikatorrør og signalforsterkere som er bildedannende.
Når gammastrålen fra en radioaktiv isotop treffer NaI-krystallen vil den bremses opp og noe av energien avgis som et lysglimt. Fotomultiplikatorrøret omdanner lysglimtet til elektriske signal som forsterkes opp via signalforsterker og omdannes til bilde. Ved å rotere rundt et objekt og ta planare bilder i ulike posisjoner (tomografere), kan man rekonstruere disse dataene til snitt gjennom objektet og få dannet en 3D-fremstilling.
Positronemittere og stråleprinsipp
PET står for Positron Emission Tomography, der en PET-skanner registrerer radioaktivitet fra positronemitterende radionuklider. Det karakteristiske ved en positronemitter er at positroner (positivt ladede elektroner) sendes ut (emitteres) fra en ustabil kjerne i et atom, f.eks. 18F (Fluor) eller 68Ga. Det vekslevirker med omkringliggende vev, positronet går bare 1-3 mm før det støter på et negativt ladet elektron i vevet og det skjer en annihilasjon (sammensmelting). All energi overføres til to fotoner (gammakvanter, lysglimt, signaler) med energi på 511 KeV som går i 180o retning i forhold til hverandre samtidig.
En PET-skanner har tusenvis av små detektorer (ca. 4 x 5 cm) tett i tett i en 360 graders ring i Gantry. Det er flere detektorringer ved siden av hverandre i en bredde på 16,21 eller 26 cm som også er bredden på et bed-opptak i pasientens lengderetning. Detektorringen registrerer de to 511 KeV gammastrålene, og en tidsforskjell i signalene gir informasjon om hvor på linjen mellom de to registreringene signalene kommer fra. Strålingen kan lokaliseres tilbake til et punkt i kroppen ved hjelp av flere koordinater. Hele pasienten kan avbildes under ett ved å ta flere bed-opptak etter hverandre samtidig som benken flytter seg inn i Gantry. Ut fra disse opptakene kan man rekonstruere snittbilder gjennom pasienten i ulike plan.
CT-avbildning i tillegg til PET-avbildning, gir ytterligere forbedring av undersøkelsen. Oppbremsing av radioaktiv stråling er den samme som for røntgenstråling, og ulik for ulike typer vev og knokler. Man bruker derfor CT-bildene som signalkorreksjon i PET-bildene. Ved å fusjonere PET og CT vil CT–bildene gi et anatomisk kart som lokaliserer nøyaktig hvor PET-funnene er. I de fleste tilfeller utføres diagnostisk CT med intravenøs kontrast i forbindelse med 68Ga-DOTATOC PET/CT-undersøkelsen (2).
Ny PET/CT skanner
Vår nye PET/CT-skanner fra 2017 er digital, og lyssignalene som registreres gjøres direkte om til elektriske signaler. Skanneren har en mye høyere tellerate og forkaster ikke data på samme måte som analoge skannere. Den har dermed mye høyere oppløselighet og kan registrere svulster ned til få millimeter. En PET/CT-skanner kan brukes til avbildning med alle typer positronemittere (f.eks. 18Fluor, 15Oksygen, 11Carbon, 68Gallium) bundet til ulike legemidler (farmakon) som gir fremstilling av ulike metabolske prosesser og sykdomstilstander i organismen. Vi følger anbefalinger fra EANM (European Association of Nuclear Medicine) Guidelines for utføring av undersøkelser (3).
Nytt radiofarmakon
Et radiofarmakon må være stabilt og ikke påvirkes kjemisk av andre stoff i kroppen. Det finnes mange forskjellige radiofarmaka med ulike biokjemiske og metabolske bindinger ut fra hva man ønsker fremstilt.
Tidligere benyttet vi radiofarmakon 111In (Indium) – Octreoscan, som vi fikk fra utlandet med flytransport. Forsinkelser oppstod iblant og pasient og personale måtte vente på leveranser til ettermiddag eller neste dag, og pasienten fikk en ekstra undersøkelsesdag.
68Ga-DOTATOC [68Ga]-DOTA-D-Phe(1)-Tyr(3)-Octreotide (SomaKit) består av en chelator/«bindestoff» (DOTA-) som er bundet til åtte aminosyrer, og vil vise opptak i somatostatinreseptor positivt vev ulike steder i kroppen (4). Sammenlignet med Octreoscan har radiofarmakonet 68Ga-DOTATOC en betydelig høyere spesifikk binding til somatostatinreseptorene (særlig SSR2 og 5) som uttrykkes i nevroendokrint svulstvev.
Vi har vurdert flere muligheter for egnet radiofarmakon. Det er mulig å kjøpe ferdig produsert radiofarmakon fra utlandet merket med en mer langlivet isotop, som 64Cu -DOTATOC, der 64Cu (kobber) har halveringstid (T1/2) på 12,7 timer. Et annet alternativ er å produsere 68Ga-DOTATOC der 68Ga har T1/2 = 68 minutter. 68Ga kan fremstilles på to måter, enten fra en syklotron eller generatorbasert, som vi har valgt. Dermed kan vi gjøre det selv og står fritt til selv å bestemme når vi utfører 68Ga-DOTATOC-PET relatert til annen aktivitet.
68Ge-/68Ga-generator – GalliAD
Inntil nylig var 68Ge-/68Ga-generatorer relativt komplisert i bruk og krevde ekstra skjerming mot stråling til omgivelsene. Våren 2018 fikk en ny og bedre skjermet generator markedstillatelse i Norge, og vi søkte om utvidet bruks- og utslippstillatelse av 68Ga til Direktoratet for Strålevern og Atomsikkerhet (DSA) for å kunne starte opp.
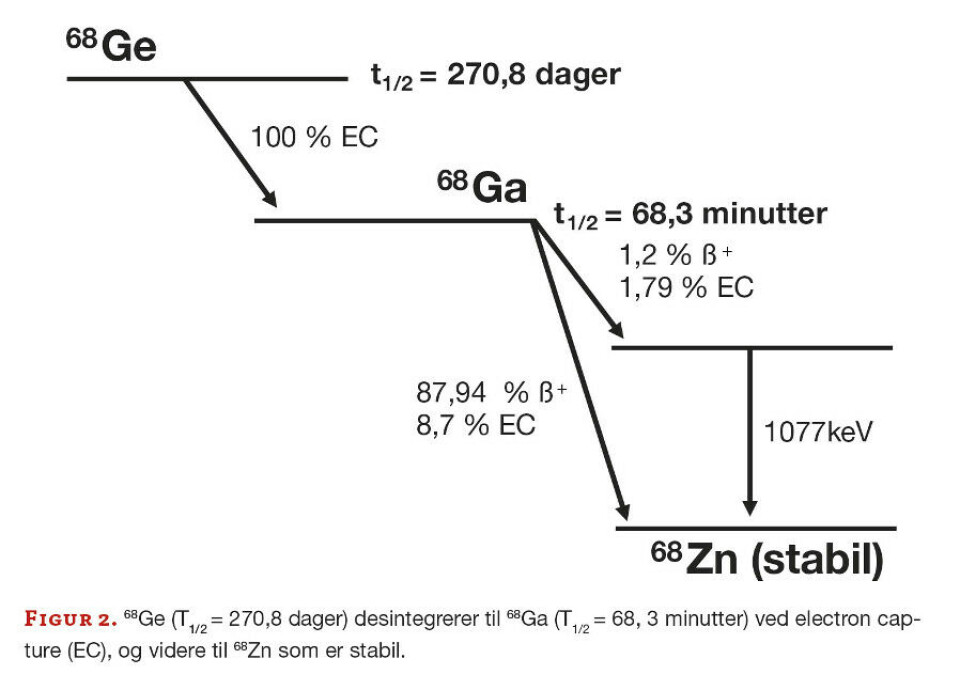
Prinsippet med en slik generator er at den har en kolonne med en fastsatt modernuklide – i dette tilfellet 68Ge (Germanium) med T1/2 på 270,8 dager. 68Ge vil desintegrere kontinuerlig og det dannes 68Ga (figur 2). Ved eluering åpner man for HCl som går inn i kolonnen, reagerer kjemisk med 68Ga og danner 68Ga-klorid (5, 6).
Generatoren er et lukket system (figur 3), og det kommer ut et fast volum saltsyre (HCl) for hver radioaktiv dose man eluerer. Generatoren inneholder totalt 610 mL HCl, som rekker til 450 elueringer (melkinger), noe som er nok til generatorens levetid på ett år. Mengde 68Ga man får ut (utbytte) vil avta over tid. Det vil si at man får mindre radioaktivitet per eluering etter hvert som generatoren blir eldre. Etter ni måneder er utbyttet redusert til 50 % (5).

Etter en eluering vil det bygge seg opp mer 68Ga på grunn av den kontinuerlige nedbrytningen av modernukliden 68Ge. Det vil ta minst syv timer etter forrige eluering før den er i ekvilibrium og gir full avkastning. Man kan imidlertid eluere på nytt etter tre timer da det har bygd seg opp 84 %. Vi praktiserer å vente fire timer mellom elueringene, noe som gir 91 % av full oppbygging av 68Ga. Har det gått ≥ 72 timer siden siste eluering, må man forkaste en eluering før man tar ut nytt eluat til bruk for innmerking. Dette skyldes fare for gjennomslag av 68Ge som på grunn av den lange halveringstiden, ikke må injiseres i pasienten. Tilsvarende vil det kreve tre påfølgende elueringer om generatoren ikke har vært brukt på en måned (5).
Innmerking - 68Ga-DOTATOC - Somakit
Det finnes kommersielle tørrstoffkit (68Ga-DOTA-TOC, 68Ga-DOTA-NOC, 68Ga-DOTA-TATE) som er enkle å merke. Disse binder seg i ulik grad til somatostatinreseptorene (SSR 1–5) på celleoverflaten.
Med den nye generatoren har vi enkelt kunne etablere egen produksjon av 68Ga-DOTATOC på vår hotlab, uten å gjøre store og dyre ombygginger. Opplæring av personalet gikk greit da vi har kunnskap og erfaring med innmerking av tørrstoffkit fra før. Daglig utfører vi innmerking in vitro med 99mTcO4- (pertechnetat) fra en Molybden/Technesium-generator til andre nukleærmedisinske undersøkelser, og 68Ga-innmerkingen følger de samme prinsippene.
Fremgangsmåte
Ved hjelp av en vakuumflaske trekker man det radioaktive 68Ga-kloridet ut fra generatoren og over i en ampulle med farmaka i form av tørrstoff (DOTATOC), som på forhånd er tilsatt buffer og sterilt H2O. Den kjemiske reaksjonen krever at det hele varmes til 95º C i syv minutter, for deretter å avkjøles. Da 68Ga har kort T1/2 og mengde radioaktivitet reduseres fort, er det viktig at innmerking og kvalitetskontroll skjer direkte etter eluering. Innmerkingsprosedyre og påfølgende kvalitetskontroller tar nesten en time.
Kvalitetskontroll av innmerking og kolloider
Det kan skje feil under innmerkingsprosessen som påvirker sluttresultatet. Innmerkingsprosent skal være svært høy for at ikke fritt 68Ga, som har annen biokjemisk bindingsmekanisme enn DOTATOC, skal binde seg til andre steder i kroppen og gi falske positive resultater. Vi benytter silikonerte kanyler under innmerking da direktekontakt med metall forurenser preparatet. Væsken må heller ikke komme i kontakt med gummiproppen i tørrstoffampullen, det fører til forurensning av sink og evt. andre metaller og det danner seg kolloider (ørsmå partikler), som også har andre bindingsmekansimer enn DOTATOC.
Kvalitetskontroll utføres ved hjelp av Thin Layer Chromatography (TLC) (figur 4), og hvis resultatene ikke er innenfor gitte grenser forkastes preparatet.
10 µL av preparatet appliseres på to ulike PH-strips som skal vise en PH mellom 3,2 og 3,8. Ved avvik kan det ha kommet ut for lite eller for mye HCl ved elueringen. Videre appliseres en dråpe på hver av to kromatografistrips som er oppmerket med en blyantstrek 1 cm fra bunn (start) og en blyantstrek 9 cm fra denne (stopp). Stripsene plasseres i hvert sitt glasskar (med hhv Na-citrat og Ammoniumacetat/Metanol som mobil fase) med en pinsett. Stripsene må ikke tas på med fingrene eller komme borti glassveggen. I karet med Na-citrat tar det cirka 5 minutter til stoppstreken nås, og i karet med Ammoniumacetat og Metanol tar det cirka 20 minutter.

Ved hjelp av en probe måles mengde gammastråler fordelt på kromatografistripsen. TLC-skanneren er koblet til et dataprogram som fremstiller avlesningen grafisk og i tillegg regner ut prosentfordeling mellom bundet og fritt 68Ga. Den viser også om det er kolloider i det ferdige preparatet som indikerer forurensning bundet til 68Ga (4).
Med Na-citrat som mobil fase sjekker man andelen fritt 68Ga i preparatet, som skal være ≤ 2 % (figur 5A). Fritt 68Ga vil vandre lenger enn det som er bundet til DOTATOC. Retensjonsfaktoren (Rf) sier noe om hvor godt den aktuelle komponenten har vandret med mobilfasen, og skal være innenfor gitte grenser (fritt 68Ga 0,9 – 1, merket 68Ga 0,1 – 0,2).
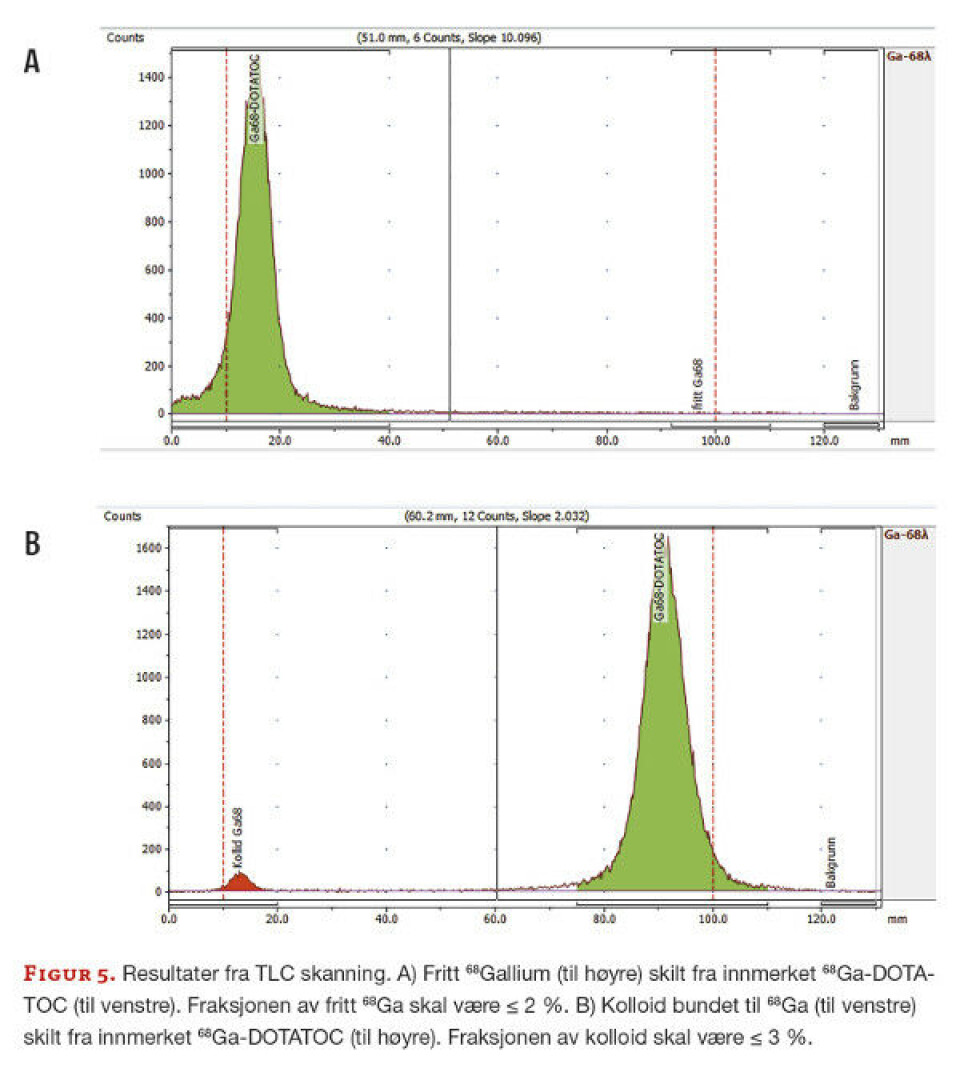
Med Ammoniumacetat/Metanol som mobil fase undersøker man om det er dannet kolloider forårsaket av forurensning i preparatet (figur 5B). Kolloidet viser seg da som partikler som vandrer kortere enn 68Ga-DOTATOC, og skal være ≤ 3 %. Rf for kolloid 68Ga er 0 - 0,1 og Rf for merket 68Ga er 0,8 – 1.
Pasientforberedelse
Pasienten skal den siste uka før undersøkelsen ikke ta langtidsvirkende Sandostatin og Ipsyl. Pasienten skal heller ikke ta korttidsvirkende av de samme preparater på selve undersøkelsesdagen. Disse preparatene blokkerer for SST-reseptoropptak av 68Ga-DOTATOC og vi får falskt for lavt opptak i svulstvevet.
Bildetaking
En time etter injeksjon av 68Ga-DOTATOC avbilder vi pasienten fra skalletopp til midt på låret. Vi kan tilpasse opptaket over lunger og øvre del av lever der det er mye bevegelse pga. respirasjon, ved å koble på et pustegatingsystem. Bildeopptakene deles opp i ulike intervall etter pasientens pustesyklus. Man velger ut bilder i samme fase av pustingen og får dermed et stillbilde, et «frosset bilde» uten bevegelse, som gjør at eventuelle opptak i svulster blir mer avgrensede og skarpere. Uten denne teknikken vil opptaket bli mer utydelig og «smøres» utover svarende til pustebevegelsene. Vi kan også stille inn ulik opptakstid over ulike deler av kroppen tilpasset behov for ønsket bildekvalitet.
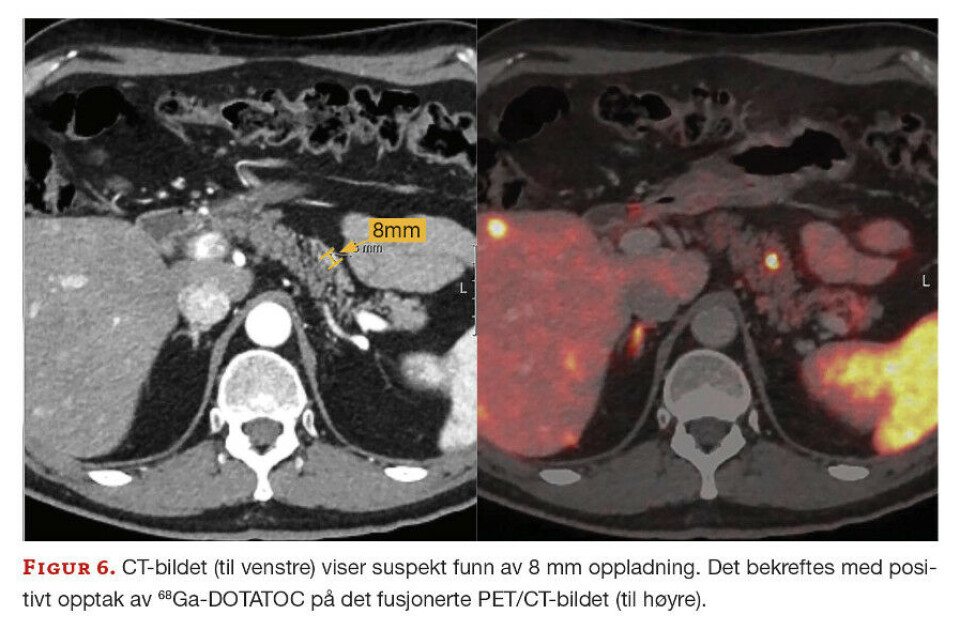
Figur 6 viser en pasient med kjent spredning av NET til lever, men ukjent opprinnelse. Pasienten har vært til gjentatte MR- og CT-undersøkelser uten å finne primærsvulst. Ved bruk av 68Ga-DOTATOC PET fant man en 8 mm nevroendokrin svulst i bukspyttkjertelen. Man ser en suspekt oppladning på CT (i venstre bilde) som bekreftes med positivt opptak av 68Ga-DOTATOC på PET-bildene til høyre, som da viser funn av nevroendokrint vev.
Feilkilder
Betennelsesvev er mer metabolsk aktivt enn normalt vev og har SST-reseptorer på overflaten. Betennelsesvev vil derfor kunne ta opp 68Ga-DOTATOC. Tettheten av reseptorer er imidlertid lavere enn i nevroendokrint vev og dermed får man et mindre intenst opptak.
I en case report ble det presentert en pasient med diffuse symptomer som lett redusert allmenntilstand og tretthet. Pasienten fikk utført en 68Ga-DOTATOC PET som viste økt opptak i hodet av bukspyttkjertelen (7). Det var mistanke om nevroendokrin svulst i bukspyttkjertelen, men det samstemte ikke med blodprøveverdier og kunne ikke bekreftes med andre undersøkelser som CT og MR. Man konkluderte med at det var normalt opptak i bakre del av hodet på bukspyttkjertelen (processus uncinatus). Senere er det dokumentert at dette området av bukspyttkjertelen normalt har et relativt høyt uttrykk av SST-reseptorer og skiller seg fra øvrige deler av bukspyttkjertelen med en annen embryologisk opprinnelse og vil dermed naturlig ha høyere opptak av 68Ga-DOTATOC.
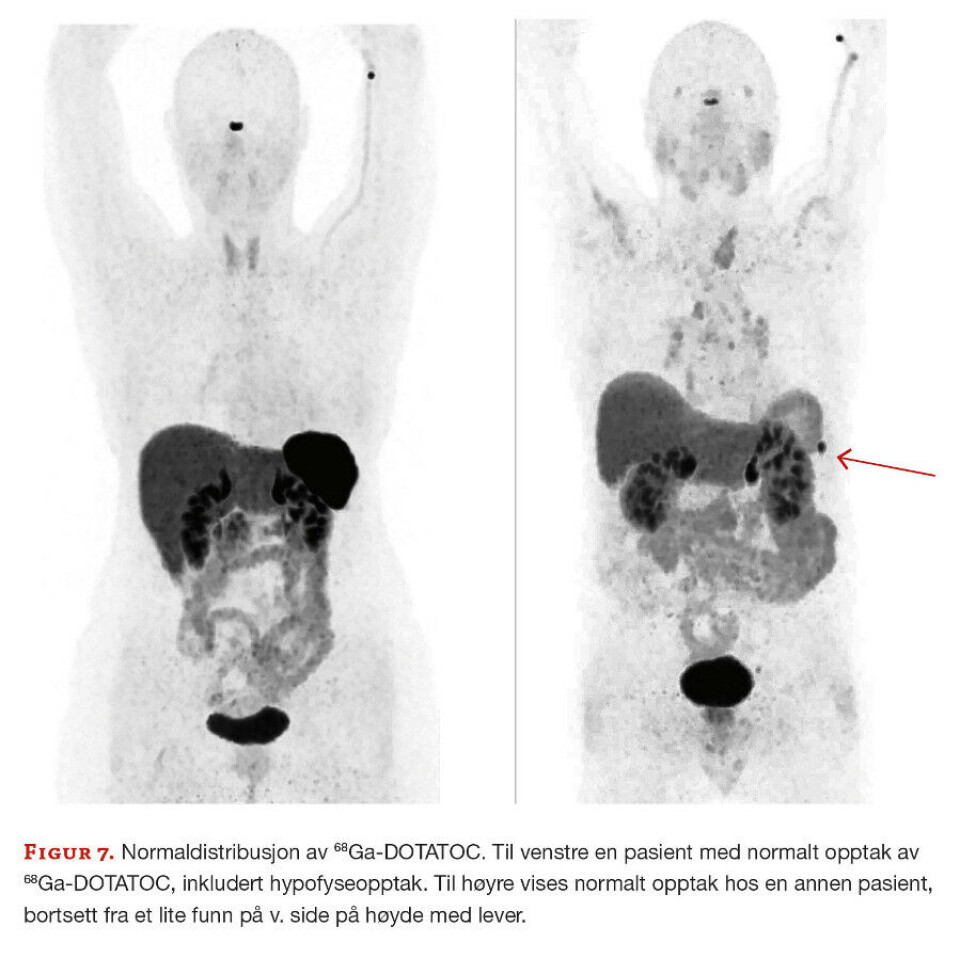
Generelt varierer normalt opptak i ulike organer og vev fra person til person, slik figur 7 illustrerer. Nukleærmedisiner som tolker bildene, må kjenne til hvordan det enkelte radiofarmaka distribueres i organismen for å kunne tolke bildene riktig.
Teranostikk – kombinert diagnostikk og terapi
Når vi nå har en målrettet avbildningsmetode med god bildekvalitet og oppløsning er veien til behandling kort. Ved å erstatte positronemitteren 68Ga bundet til DOTATOC med 177Lu (Lutetium) som er en behandlende radionuklide (β-emitter) (177Lu-DOTATATE), kan man behandle pasienten og man vet allerede hvor behandlingen tas opp. β-stråler går kun noen millimeter før de vekselvirker med omkringliggende vev og gir behandlingseffekt (8).
Dette behandlingstilbudet har vært tilgjengelig i utlandet i mange år, og fra høsten 2019 ble det etablert på Haukeland Universitetssjukehus og Oslo Universitetssykehus.
Det benyttes ulike typer behandling for denne pasientgruppen avhengig av utbredelse, symptomer og hvor i sykdomsforløpet pasienten er. Kirurgi er eneste mulighet for kurasjon. Ofte har sykdommen pågått lenge før den metastaserer og endrer karakter, og først da blir oppdaget. Øvrig behandling kan være medikamenter som blokkerer for SST-reseptoren eller for ulike signalveier, eller cytostatika, strålebehandling og 177Lu-DOTATATE som kan bremse og stoppe videre sykdomsutvikling (9). Behandlingsopplegget skreddersys til den enkelte pasient avhengig av utbredelse av sykdommen, hvilke organsystem som er påvirket, symptomer og allmenntilstand.
Oppsummering
Etableringen av 68Ga-DOTATOC PET/CT har vært en lang prosess. Vi har hatt nytte av å hospitere ved Senter for nukleærmedisin/PET på Haukeland Universitetssjukehus (som etablerte metoden høsten 2017), samt deltakelse på Europeisk kongress i Nukleærmedisin (Düsseldorf, høst 2018) hvor vi så på nødvendig utstyr fra ulike leverandører. I tillegg har vi jobbet tett med leverandøren av generatoren for praktisk tilrettelegging og opplæring. De var også til stede under vår første pasientundersøkelse. Bildene vi nå fremstiller på PET/CT-skanneren er av høy kvalitet, og de kan knapt sammenlignes med bildene kjørt etter gammel metode med SPECT/CT.
Takk
Jeg vil rette en stor takk til Mona-Elisabeth Revheim, overlege og seksjonsleder for legene ved Nukleærmedisin OUS. Hun har bidradd med det medisinske aspektet og hjulpet meg med forklaring rundt nevroendokrine svulster, inkludert noen pasientkasuistikker.
Så vil jeg takke SamNordic, Sverige som markedsfører både GalliAD og Somakit og som har gitt meg tillatelse til å bruke informasjon fra deres prosedyrer og manualer.
Takker også velvillige kollegaer ved Nukleærmedisin Rikshospitalet som har lest gjennom artikkelen og kommet med innspill og rettelser underveis.
Nukleærmedisinen trenger både bioingeniører og radiografer
























