FAG i praksis
Hiv-diagnostikk – riktig valg av test
I diagnostikk av hiv-infeksjon benyttes både serologi og molekylærgenetikk. Hvilke tester har vi, og ved hvilken indikasjon skal de ulike testene benyttes?
Hiv-diagnostikk - riktig valg av test.pdf(241 KB)
En hverdag på ”Hiv-plassen”
Det er mandag, arbeidsdagen på PCR-laboratoriet har startet, og bioingeniør Kari tar fatt på ”Hiv-PCR plassen”. Dagens første bunke med prøver og rekvisisjoner ligger på arbeidsbenken. Kari kobler prøve opp mot rekvisisjon og gjør samtidig noen vurderinger. Hva slags prøvemateriale er mottatt? Når er prøvene tatt?

Det første prøverøret er EDTA fullblod uten gel tatt før helgen med ønske om kvantitering av hiv RNA. ”Typisk”, tenker Kari, litt oppgitt, og noterer ”avvist på grunn av for lang forsendelsestid”. Neste prøve med ønske om samme test blir dessverre også avvist. Det er et usentrifugert EDTA gelrør, tatt fredag. ”Hadde de bare sentrifugert røret før forsendelse”, sier hun til seg selv og blar videre i bunken av rekvisisjoner. Den største mengden kommer fra infeksjonsmedisinske poliklinikker. Alle er pasienter med kjent hiv-infeksjon og registreres derfor fortløpende på hiv RNA kvantitering. Noen av rekvirentene ønsker også hiv-resistens. Kari registrerer dette.
Neste prøve i rekken er et serumrør. På rekvisisjonen står det kun ”status”, og det er krysset av for både hiv DNA Provirus og hiv RNA-kvantitering. Kari stusser fordi det kun er mottatt serum, og ikke EDTA fullblod og plasma som ønskelig. Det er dessuten uvanlig at rekvirenten har krysset av for begge testene. Kari mistenker at rekvirenten egentlig ønsker serologisk undersøkelse. Hiv RNA kvantitering utføres jo kun på pasienter med kjent hiv-infeksjon, og hiv DNA Provirus er i hovedsak en test som benyttes når serologi ikke er tilstrekkelig. Kari finner ingen tidligere prøvesvar på pasienten og konfererer derfor med medisinsk ansvarlig på laboratoriet. Det viser seg at pasienten ikke har en kjent hiv-infeksjon. Det er heller ikke snakk om smitte, men kun et ønske om status. Resultat: Det er ikke indikasjon for PCR, og prøven sendes til screening med serologi.
Kari tar fatt på enda en bunke med prøver. På den første rekvisisjonen står det ”Ubeskyttet sex i utlandet” og ønsket test er hiv DNA Provirus. Kari tenker; ”hvor lenge er det mellom antatt smittetidspunkt og prøvetakningstidspunkt i dette tilfellet? Er tidsrommet over 15 dager er jo serologi bedre egnet enn provirus”. Hun sjekker pasienten i laboratoriedatasystemet, konfererer med medisinsk ansvarlig og sender prøven til serologilaboratoriet. Det viser seg nemlig at smitteeksponeringen skjedde mer enn tre uker før blodprøven ble tatt. Riktig førstevalg her er serologisk undersøkelse, ikke PCR.
Lenger nede i bunken finner hun en EDTA fullblodprøve med ønske om hiv DNA Provirus. «Usikker serologi» er oppgitt i rubrikken «Kliniske opplysninger».
Usikker serologi er en av de vanligste indikasjonene for hiv DNA Provirus, så her er det ingen tvil. Kari sjekker prøverøret og ser at prøven er kommet innen fristen på tre dager. ”Endelig en pasientprøve hvor alt stemmer”, tenker hun.
Over til serologilaboratoriet
Rett rundt hjørnet, på serologilaboratoriet, er bioingeniør Ola i gang med hiv-screening. Prøvene som Kari har sendt videre fra PCR-laboratoriet har kommet og er med i maskinen. Prøvesvarene sendes ut senere på dagen, om enn litt forsinket.
Ola har mye å gjøre. De aller fleste prøvene med ønske om hiv-status blir nemlig først screenet med serologi. I dag er det både prøver med ønske om immunstatus, og prøver fra pasienter som har vært i mulig risikosituasjon. I tillegg screenes gravide og blodgivere for hiv. Maskinen går for fullt, og Ola vurderer svarene fortløpende.
Et svakt reaktivt resultat på en av prøvene får ham til å reagere. Pasienten har ingen kjent hiv-infeksjon og det er heller ikke oppgitt noen kliniske opplysninger. Prøven sentrifugeres og analyseres på nytt i parallell. Den er fremdeles svak reaktiv. Er dette en helt nyoppdaget hiv-infeksjon eller bare noe uspesifikt? Ola bestiller konfirmasjonstesten hiv Western Blot.
Neste screeningprøve Ola vurderer har også et svakt reaktivt resultat. Når denne prøven analyseres på nytt i parallell etter sentrifugering, blir begge parallellene negative. Her var det tydeligvis noe uspesifikt som gjorde utslag i testen, og Ola besvarer prøven som negativ.
Ola får stadig nye prøver som er ferdig registrert og klare til å settes inn i maskinen. De fleste er negative, men en prøve har et sterkt reaktivt resultat. Han sjekker i laboratoriedatasystemet, og ser at pasienten er innlagt på sykehuset, men finner ingen tidligere prøvesvar. Ola konfererer med medisinsk ansvarlig som ringer avdelingen. I følge behandlende lege har ikke pasienten kjent hiv-infeksjon, men funnet kan stemme med sykdomsbildet. Ola bestiller hiv Western Blot for å bekrefte funnet i screeningtesten.
Ola er i ferd med å avslutte for dagen. Før han går, finner han frem prøvene til hiv Western Blot-oppsettet dagen etter. De fleste er fra pasienter som har fått reaktiv screeningtest og som ikke har tidligere kjent hiv-infeksjon. Kontrollprøver fra pasienter med tidligere usikker hiv-serologi, tas også med. I tillegg finner han frem tilsendte prøver som andre mikrobiologiske laboratorier har screenet og funnet reaktive. Disse analyseres alltid direkte med hiv Western Blot.
Referanselaboratoriet for hiv
Kari og Ola, våre oppdiktede bioingeniører, kunne jobbet ved Avdeling for Mikrobiologi ved Oslo universitetssykehus, Ullevål. Avdelingen er referanselaboratorium for hiv i Norge, og referansefunksjonen er lagt til Enhet for Molekylærdiagnostikk og virologi, Enhet for infeksjonsserologi og Seksjon for utvikling. Arbeidet Kari og Ola gjør denne dagen, gir et innblikk i vår hverdag med hiv-diagnostikk.
Hovedtyngden av prøver til hiv-testing går til serologisk screening med fjerde generasjon hiv-antigen/antistoff kombinasjonstest (cirka 70 000 tester per år) og til hiv-1 RNA kvantitering for pasienter med allerede påvist hiv-infeksjon (cirka 6000 tester per år). I tillegg utføres ulike tester for videre utredning og oppfølging av pasientene.
Vi skiller mellom tester som benyttes i primærdiagnostikk, det vil si for å avklare hvorvidt en pasient har hiv-infeksjon eller ikke, og tester som benyttes i oppfølging av pasienter med kjent hiv-infeksjon (se tabell 1 nederst). Denne artikkelen beskriver testene som vi - som referanselaboratorium - benytter i primærdiagnostikk av hiv.
Hiv kombinasjonstest
Hiv antigen/antistoff kombinasjonstest, er et enzyme immunoassay (EIA) som påviser både hiv-antigen og hiv-antistoff. Antigenet som påvises er p24, et protein i kappen til viruset. Antistoffene som påvises er rettet mot antigener i membranen til henholdsvis hiv type 1 og hiv type 2. Antigenene som er brukt i testen er rekombinante eller syntetiske. Det benyttes flere ulike antigener for å sikre at testen fanger opp subtyper av viruset (2). Testen kan påvise både IgM - og IgG -antistoffer, og dermed fange opp antistoffrespons tidlig etter serokonversjon når antistoffdannelsen starter i kroppen.
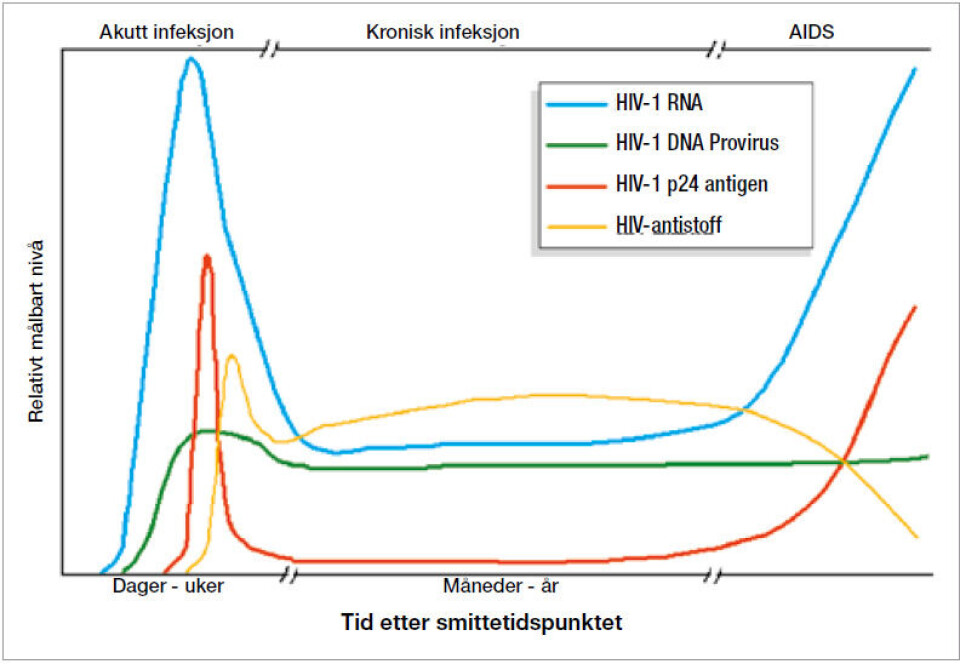
I de aller fleste tilfeller er hiv kombinasjonstesten den første testen som utføres ved spørsmål om hiv-infeksjon. At antigen kan påvises i tillegg til antistoff, gjør at hiv kombinasjonstesten er mer sensitiv enn rene antistofftester den første tiden etter smitte, før antistoffdannelsen har kommet skikkelig i gang (se figur 1 nederst). I noen tilfeller kan testen påvise hiv-smitte allerede én til to uker etter smittetidspunkt (2). Hiv kombinasjonstesten benyttes også til screening av blodgivere og gravide.
Testen har god diagnostisk og analytisk sensitivitet, noe som er ønskelig for å minimere risikoen for falske negative resultater. Imidlertid kan det i en svært sensitiv test forekomme uspesifikke reaksjoner. Falske positive reaksjoner er sett ved infeksjon med andre agens, men sammenhengen er ikke alltid tydelig (3). Ofte skyldes det tilfeldige kryssreaksjoner. I forbindelse med svangerskap er det ikke sjeldent at slike forbigående uspesifikke reaksjoner forekommer (4). Konfirmerende tester og kontrollprøver vil avklare om reaktiviteten i hiv kombinasjonstesten er uspesifikk.
Hiv kombinasjonstesten har høy negativ prediktiv verdi. Ved screening og ønske om immunstatus uten mistanke om smitteeksponering, er det derfor ikke behov for kontrollprøve når hiv kombinasjonstesten er negativ. En negativ test kort tid etter smitteeksponering bør derimot følges opp med en kontrollprøve etter fire til åtte uker og etter tre måneder. Dersom prøven er tatt tidlig i forløpet, kan den være negativ selv om pasienten er smittet. Da er det verken antigener eller antistoffer å påvise i blodet og testen blir følgelig negativ. Infeksjonens forløp kan variere, men for de aller fleste smittede, vil testen bli reaktiv innen seks til åtte uker etter smittetidspunktet. Etter tre måneder er vindusfasen godt dekket, og en negativ test vil utelukke hiv-smitte dersom det ikke har vært ny smitteeksponering i mellomtiden.
Hiv Western Blot
Med hiv-1 Western Blot kan man påvise tilstedeværelse av spesifikke antistoffer mot de enkelte hiv-1 antigenene. Antistoffene kommer frem som bånd på nitrocellulosestriper. Antigenene i testen er både fra membranen (env), kappen (gag) og kjernen (pol) til viruset. Med hiv-1 Western Blot kan man påvise antistoffrespons mot alle varianter, subtyper og grupper av hiv-1 som er kjent i dag (2). I Norge er det anbefalt å benytte hiv Western Blot til konfirmering av reaktive screeningtester (2).
I omslagsfasen hvor pasienten er i ferd med å serokonvertere, er båndmønsteret ofte ufullstendig. De første antistoffene som påvises er rettet mot overflaten av viruset. Deretter vil det i takt med infeksjonsforløpet dannes antistoffer mot stadig flere hiv-1 antigener. Båndmønsteret i testen utvikles til et fullstendig mønster med antistoffer mot alle de tre gruppene antigener (se figur 2 nederst). Ved gradvis økende immunsvikt, som også påvirker evnen til å danne antistoffer, vil noen av båndene forsvinne. Med hiv Western Blot kan man dermed ikke skille mellom en hiv-infeksjon i tidlig fase og langtkommet immunsvikt. Uspesifikke reaksjoner kan også forekomme og ses ofte som et enkelt bånd (3).
Ved ufullstendig båndmønster vil en kontrollprøve etter to til tre uker som regel avklare spørsmålet om hiv-infeksjon eller uspesifikk reaksjon. I den tidlige fasen av en hiv-infeksjon, vil man alltid se en utvikling i båndmønsteret. Manglende utvikling støtter konklusjonen om uspesifikk reaksjon, men også ved langtkommen immunsvikt vil mønsteret kunne være uendret. Ofte kan det være aktuelt å supplere med hiv-1 antigentest med nøytralisasjon eller hiv-1 DNA Provirus PCR for nærmere avklaring.
Et negativt hiv-1 Western Blot alene er ikke tilstrekkelig for å utelukke hiv-infeksjon ved reaktiv hiv kombinasjonstest. Det bør alltid tas en kontrollprøve etter to til tre uker. Med hiv-1 Western Blot kan man bare påvise IgG-antistoffer, ikke antigen eller IgM-antistoffer, og testen kan derfor være negativ ved akutt infeksjon. Hiv-infeksjon kan først utelukkes etter at kontrollprøven er undersøkt.
Hiv antigentest
Siden hiv kombinasjonstesten påviser både antigen og antistoff, og hiv-1 Western Blot bare påviser antistoff, kan det være nyttig med en egen test for hiv-1 antigen. Hiv-1 antigentesten er en EIA-test som påviser p24-antigenet fra kappen til hiv-1. For å konfirmere en positiv hiv-1 antigentest, utføres nøytralisasjon. Hiv-1 antigentesten benyttes ved inkonklusivt hiv-1 Western Blot og mistanke om akutt hiv-infeksjon. I disse tilfellene er også hiv-1 DNA Provirus PCR aktuelt. PCR har bedre sensitivitet, men fordelen med hiv-1 antigentesten er at den kan utføres i samme prøve som ble reaktiv i kombinasjonstesten.
Hiv-1 antigentesten kan ikke alltid gi en sikker konklusjon. I omslagsfasen hvor pasienten er i ferd med å serokonvertere, kan det dannes immunkomplekser av antigen og antistoff slik at antigenene ikke kan påvises i testen. I den kroniske fasen av en hiv-infeksjon kan virusmengden være så lav at antigentesten er negativ (figur 1). Uspesifikke reaksjoner forekommer også, men disse kan som regel identifiseres ved at de ikke lar seg konfirmere med nøytralisasjon.
Hiv-2 diagnostikk
Hiv-2 infeksjon er lite utbredt i Norge, men det anbefales likevel at man benytter et hiv-1 Western Blot som inneholder et hiv-2-spesifikt peptid. Ved utslag i hiv-2 båndet og mistanke om hiv-2 infeksjon, analyseres prøven på et spesifikt hiv-2 Western Blot hvor man kan påvise antistoffer mot de enkelte hiv-2 antigenene.
Hiv hurtigtester
Det finnes flere hiv hurtigtester. De fleste påviser hiv-1 og hiv-2 antistoff, men det finnes også tester som kan påvise antigen. Hurtigtestene benytter immunkromatografi som er en mindre sensitiv metode enn EIA, og vindusfasen er noe lenger for hiv hurtigtester enn for EIA kombinasjonstester. Hiv hurtigtester kan også gi falske reaktive resultater. De kan likevel ha stor nytteverdi i pasientnær diagnostikk hos definerte risikogrupper (5). Uansett resultat på en hiv hurtigtest, skal det alltid samtidig tas prøve til hiv kombinasjonstest (EIA).
Hiv-1/2 DNA Provirus PCR
I tillegg til serologiske tester, benyttes også molekylærgenetikk (PCR) i utredning av hiv-infeksjon. Polymerase Chain Reaction (PCR) er en metode for å amplifisere en bestemt DNA-sekvens. Provirus er per definisjon et virusgenom integrert i vertcellens DNA.
På Ullevål benytter vi en in-house konvensjonell «nested» (se under) PCR for påvisning av hiv-proviralt DNA. Med hiv DNA Provirus PCR påvises gensekvenser integrert i cellekjernen til virusinfiserte leukocytter. Prøvematerialet er derfor EDTA fullblod. Vi utfører først en automatisk ekstraksjon av DNA og deretter oppformering av DNA med multipleks nested PCR. ”Multipleks” betyr i dette tilfellet at vi oppformerer to ulike gensekvenser. ”Nested” vil si at vi benytter to PCR-oppsett etter hverandre (PCR-I og PCR-II) for hver av gensekvensene. I PCR-II oppformeres en kortere sekvens inne i sekvensen fra PCR-I-produktet.
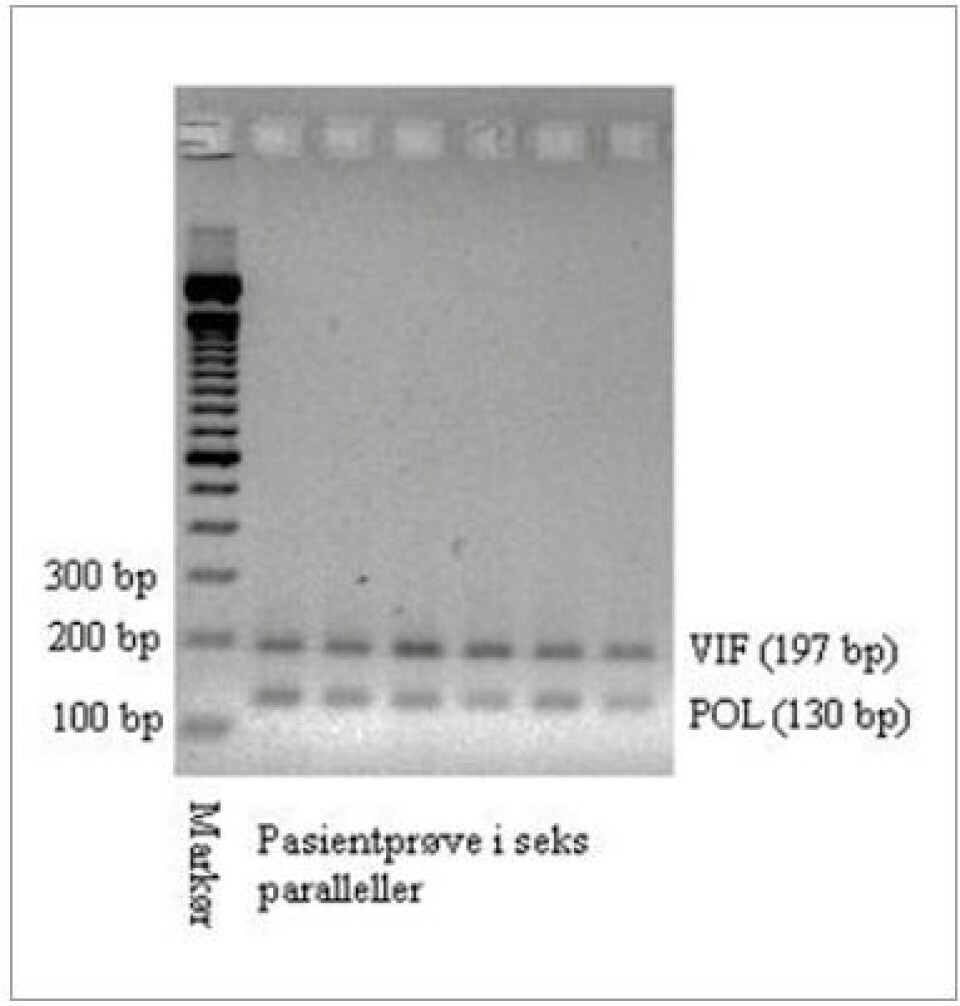
Det endelige produktet fra PCR-II påvises til slutt med gelelektroforese. Applisert PCR-produkt fra prøver og kontroller vandrer i gelen fra negativ pol til positiv pol og separeres etter størrelse. Ved endt elektroforese legges gelen i UV-kamera og de oppformerte gensekvensene blir til synlige bånd. Gensekvensene har et kjent antall basepar (bp) og vurderes opp mot en applisert markør (se figur 3 nederst).
En egen sanntids-PCR for retinoblastomgenet benyttes som internkontroll for prøvene. Retinoblastomgenet finnes i én kopi per celle. Påvisning av genet er kontroll på at vi har fått med nok leukocytter under ekstraksjonen og at prøven ikke inneholder noe som hemmer PCR-reaksjonen. Er internkontrollen negativ og tilhørende nested PCR negativ, skal prøven analyseres på nytt. Er nested PCR positiv, er det ikke nødvendig med retest ved negativ internkontroll.
Hver prøve analyseres i seks paralleller. Hos de fleste pasienter med ubehandlet hiv-1infeksjon, vil det være én hiv-1infisert celle per 1000 - 1000 000 sirkulerende leukocytter. For å fange opp minst én infisert celle, benytter vi 300 mikroliter prøvemateriale til ekstraksjon. Variasjonen i antall hiv-1infiserte celler indikerer behovet for å analysere prøven i flere paralleller. Jo flere paralleller som analyseres, desto større blir sannsynligheten for å påvise en hiv-1 infisert celle hos en hiv-1 infisert pasient. Kriteriet for en positiv prøve er minimum ett bånd på rett plass i én av parallellene.
Indikasjon for hiv DNA Provirus PCR
Hiv DNA Provirus PCR benyttes kun på spesielle indikasjoner:
- Oppfølging av barn født av mødre med kjent hiv-infeksjon.
- Inkonklusiv serologi.
- Sannsynlig reell smitteeksponering i tidsrommet 10 -15 dager før prøvetakningstidspunktet.
- Særskilte krav/retningslinjer for donorer og nedfrysning av celler og vev.
Vi utfører hiv-1 DNA Provirus PCR rutinemessig hver uke. Hiv-2 DNA Provirus PCR er ikke en rutineanalyse, men kan utføres på forespørsel.
Under svangerskap passerer mors IgG over placenta, og maternelt IgG kan påvises hos barnet fram til 18 måneders alder. Barn født av mødre med hiv-infeksjon vil ha reaktiv hiv kombinasjonstest i lang tid og disse barna må derfor følges opp med hiv DNA Provirus PCR. Det anbefales tre kontrollprøver (6). Den første prøven skal tas to til tre uker etter fødsel. De neste kontrollprøvene skal tas etter fire til seks uker og etter fire til seks måneder. Ved bruk av hiv kombinasjonstest, vil man også se et fall i antistoffnivå etter hvert som de maternelle antistoffene forsvinner. Dersom hiv DNA Provirus PCR er negativ i alle tre kontrollprøvene, er det ikke nødvendig med ytterligere kontroll og smitte fra mor til barn kan utelukkes.
Ved inkonklusiv serologi kan man supplere med hiv DNA Provirus PCR for nærmere avklaring. Påvist hiv DNA Provirus bekrefter hiv-infeksjon, men et negativt hiv-provirusresultat må alltid følges opp med kontrollprøver til serologi, da nylig smitte med hiv ikke kan utelukkes selv om hiv DNA Provirus PCR er negativ.
Hvilke tester som bør benyttes i hiv-diagnostikk etter sannsynlig reell smitteeksponering, er avhengig av tid mellom smitteeksponering og prøvetakning. I tidsrommet 10-15 dager etter smitteeksponering, er hiv DNA Provirus PCR best egnet til å påvise hiv-infeksjon. Serologisk screening vil sjelden kunne påvise hiv-infeksjon før tidligst etter 15 dager.
Valg av riktig test
Før vi analyserer en pasientprøve med hiv DNA Provirus PCR, vurderer vi om det virkelig er indikasjon for å utføre analysen. I denne sammenhengen er det viktig med relevante kliniske opplysninger. Ved mangelfulle opplysninger på rekvisisjonen, må vi se på tidligere prøvesvar og eventuelt ringe rekvirenten for å bestemme hvorvidt analysen skal utføres eller ikke.
Laboratoriet erfarer at det av og til er misforståelser om riktig bruk av tester og at indikasjon for bruk av serologiske tester og tester for agenspåvisning (PCR) forveksles. Rekvirerte tester samsvarer heller ikke alltid med kliniske opplysninger eller tidligere prøvesvar. Riktig test, riktig prøvetakning og behandling av prøven før forsendelse, er svært viktig for å kunne gi et raskt og korrekt svar. EDTA-plasma og serum er uegnet som prøvemateriale til hiv DNA Provirus PCR. Slike prøvematerialer avvises og vi ber om ny korrekt prøve av pasienten. Kun EDTA fullblod kan benyttes og prøvematerialet er holdbart i opptil tre dager.
Konklusjon
Det er viktig å være klar over forskjellen på serologisk screening og PCR, og hvilke tester som skal benyttes i ulike kliniske tilfeller. PCR er en metode som stadig ekspanderer i bruk på det diagnostiske feltet. Likevel er det ”å ta en hiv-test” fremdeles synonymt med serologi i dag. Riktig utfylte rekvisisjoner og korrekt prøvemateriale er avgjørende for en god arbeidsflyt på laboratoriet, valg av riktig test og raske prøvesvar. En hiv-diagnose stilles ved positivt hiv Western Blot eller positiv hiv-antigen test konfirmert med nøytralisasjon eller påvist hiv DNA Provirus. Like viktig som å stille en hiv-diagnose, er det å utelukke hiv-infeksjon.